Краткий конспект подготовки к ЗНО по химии №39 Белки
Белки – это природные полимеры, построенные из остатков аминокислот.
Гидролиз белков
Пептидная связь гидролизуется в кислой или щелочной среде. При этом образуются соли аминокислот по карбоксильной группе или по аминогруппе.
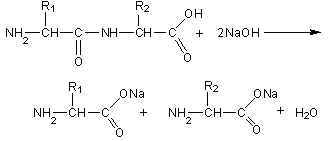
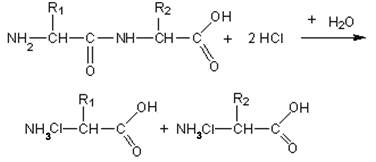
Белки гидролизуются и под действием ферментов
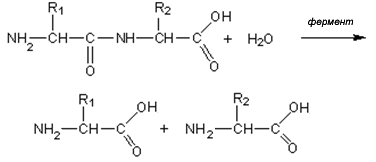
Функции белков в организме
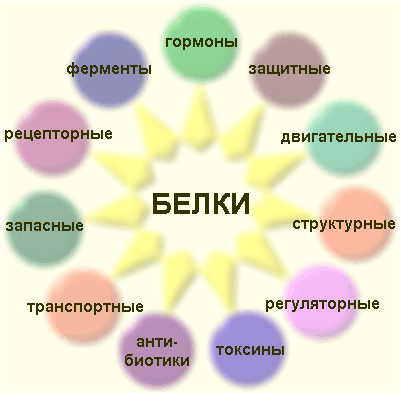
Функции белков в организме.
Строение белков
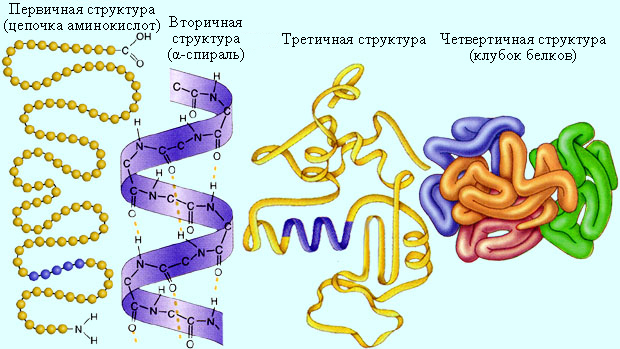
Первичная структура белка – это последовательность аминокислотных остатков.
Вторичная структура белка – расположение полипептидной цепи в пространстве, обусловленное водородными связями между атомом кислорода карбоксильной группы и атомом водорода аминогруппы разных аминокислотных остатков.
Третичная структура белка – расположение вторичной структуры в пространстве, обусловленное дополнительными взаимодействиями между различными участками полипептидной цепи.
Четвертичная структура белка – объединение нескольких полипептидных цепей в один белок.
Например, гемоглобин состоит из 4 пептидных цепочек, каждая из которых содержит по 140 остатков аминокислот.
Химические свойства белков
1. Денатурация белка
Денатурация – разрушение вторичной, третичной и четвертичной структуры белка при различных воздействиях (нагревании, действии растворителей, иногда даже при энергичном встряхивании). Первичная структура при этом не разрушается.
При снятии неблагоприятных воздействий наступает – ренатурация – восстановление до четвертичной структуры.
Деструкция – полное разрушение, затрагивающее даже первичную структуру.
Деструкция происходит при варке яйца, скисании молока.
2. Качественные реакции на белок
А. При нагревании белки разлагаются с выделением летучих продуктов, издавая характерный запах жженых перьев.
Б. Ксантопротеиновая реакция – пожелтение белка при действии концентрированной азотной кислоты (окраска появляется за счет нитрования бензольных колец, входящих в состав остатков ароматических аминокислот).
В. Биуретовая реакция – окрашивание в ярко-фиолетовый цвет при действии раствора соли меди(II) в щелочной среде – обусловлена образованием комплексов иона меди(II) с боковыми аминогруппами.











