Краткий конспект подготовки к ЗНО по химии №38 Аминокислоты
Аминокислоты – это органические соединения, молекулы которых содержат и карбоксильную группу  , и аминогруппу
, и аминогруппу  .
.
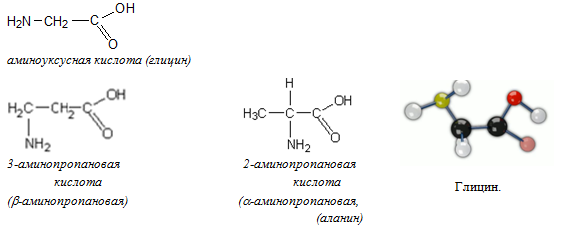
В состав белков входят только аминокислоты, в которых аминогруппа и карбоксильная группа находятся у одного и того же атома углерода (α-аминокислоты).
Общая формула природных аминокислот
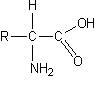
Примеры некоторых природных α-аминокислот
| Глицин |  |
Gly |
| Аланин |  |
Ala |
| Аспарагиновая кислота |  |
Asp |
| Цистеин |  |
Cys |
| Лизин |  |
Lys |
| Тирозин |  |
Tyr |
| Глутаминовая кислота |  |
Glu |
Обратите внимание, что молекулы природных аминокислот могут включать и другие функциональные группы.
Амфотерность аминокислот
Амфотерность – это способность одного вещества проявлять как кислотные, так и основные свойства.
В молекуле аминокислоты присутствуют одновременно оснóвная группа (аминогруппа) и кислотная группа (карбоксильная группа). Эти группы взаимодействуют друг с другом, как кислота с основанием, и образуется внутренняя соль:

Поэтому аминокислоты похожи по физическим свойствам на соли: это твердые, кристаллические вещества, растворимые в воде. Среда растворов нейтральная.
Все ли аминокислоты нейтральны? Строго говоря, нет. Например, раствор лизина имеет основную среду, а раствор глутаминовой кислоты – кислотную:
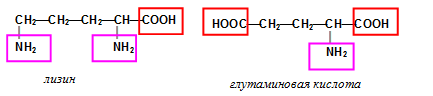
Будучи амфотерными, аминокислоты могут взаимодействовать и с кислотами, и с основаниями с образованием солей:
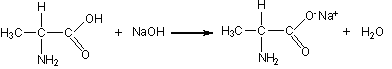
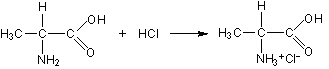
Образование пептидов
Пептидная связь – полярная ковалентная связь между атомом углерода группы  и атомом азота группы
и атомом азота группы  двух разных α-аминокислот.
двух разных α-аминокислот.
Пептид – вещество, состоящее из остатков α-аминокислот, соединенных пептидными связями.
В определенных условиях от аминогруппы одной молекулы и карбоксильной группы другой молекулы отщепляется молекула воды, и два остатка аминокислот соединяются пептидной связью:
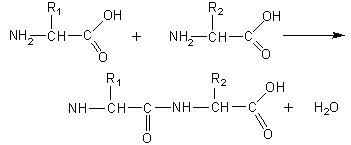
На концах получившейся молекулы (дипептида) – свободные аминогруппа и карбоксильная группа. Они могут реагировать с другими аминокислотами, образуя трипептиды, тетрапептиды… полипептиды.
Дипептид – вещество, состоящее из остатков двух аминокислот, соединенных пептидными связями.
Полипептид – полимер, состоящий из остатков аминокислот, соединенных пептидными связями.
В общем случае (не только для α-аминокислот) связь, которой соединены остатки аминокислот, носит название амидной связи. Синтетические аминокислоты применяют в промышленности для получения полиамидов, идущих на изготовление волокон и тканей. Например, всем известный полимер капрон образован из ε-аминокапроновой кислоты  :
:
Получение аминокислот.
1. Гидролиз белков
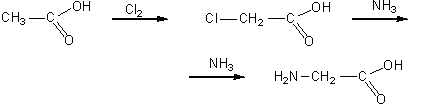
2. Получение глицина: