Краткий конспект подготовки к ЗНО по химии №27 Алкины
Алкины (ацетиленовые углеводороды) – углеводороды, молекулы которых содержат тройную связь углерод-углерод. Общая формула алкинов –  .
.
Номенклатура алкинов
Тройную связь обозначают суффиксом ин.
![]()
ацетилен (этин)
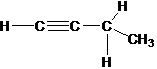
бутин-1
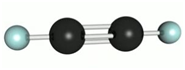
Шаростержневая модель ацетилена.
Главная цепь должна включать в себя тройные связи, а нумерация проводится так, чтобы они получили наименьшие номера.
3,6-диметилгептадиин-1,4
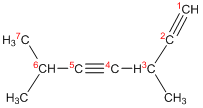
Строение алкинов
Атомы углерода тройной связи находятся в состоянии  -гибридизации. Сигма-связи, образуемые
-гибридизации. Сигма-связи, образуемые  -гибридными атомами углерода, расположены под углом
-гибридными атомами углерода, расположены под углом  друг другу.
друг другу.
Тройная связь короче и прочнее двойной связи. Она образована тремя парами электронов и включает одну σ- и две π-связи. Две π-связи лежат во взаимно перпендикулярных плоскостях.
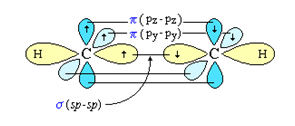
Образование тройной связи в молекуле ацетилена.
Изомерия алкинов
1. Изомерия скелета
2. Изомерия положения тройной связи
бутин-1 бутин-2
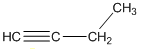
![]()
3. Межклассовая изомерия. Алкинам изомерны, например, алкадиены и циклоалкены.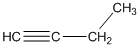
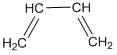
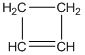
бутин-1 бутадиен-1,3 циклобутен
Алкины не обладают геометрической изомерией.
Физические свойства алкинов
Ацетилен, пропин и бутин-1 при комнатной температуре – бесцветные газы, остальные алкины – жидкости или твердые вещества.
Ацетилен немного растворим в воде, хорошо растворяется в ацетоне. Это используют для его хранения и транспортировки. Ацетилен нельзя хранить в баллонах в сжатом состоянии, т.к. под давлением он разлагается со взрывом. В баллон помещают пористый материал, пропитанный ацетоном, а в нем растворяют ацетилен.
Получение алкинов
1. В промышленности ацетилен получают термическим разложением (пиролизом) метана:
 .
.
2. Для получения ацетилена в лаборатории и в технических целях используют взаимодействие карбида кальция с водой: 
3. Другие алкины в лаборатории получают взаимодействием дигалогеналканов, содержащих атомы галогенов у одного или у соседних атомов углерода, со спиртовым раствором щелочи при нагревании:
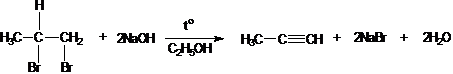
Химические свойства алкинов
1. Гидрирование алкинов.
Гидрирование алкинов протекает в тех же условиях, что гидрирование алкенов. В зависимости от количества водорода может образоваться алкен или алкан.
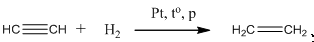
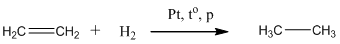
2. Галогенирование.
Обесцвечивание бромной воды – качественная реакция на алкины, так же как на алкены.
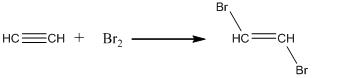
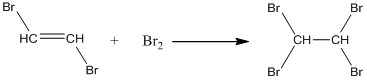
3. Гидрогалогенирование.
Присоединение хлороводорода к ацетилену приводит к образованию винилхлорида (хлорэтена) – мономера для синтеза распространенного материала поливинилхлорида (ПВХ):

4. Гидратация (реакция Кучерова)
Реакция проходит в кислой среде в присутствии солей ртути. Образующийся на первой стадии енол перегруппировывается в карбонильное соединение.
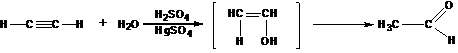
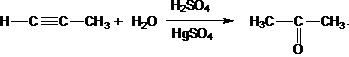
5.Окисление алкинов.
1. Обесцвечивание подкисленного раствора перманганата калия – качественная реакция на соединения с кратной связью.











