Краткий конспект подготовки к ЗНО по химии №25 Алканы. Строение молекул, номенклатура, физические и химические свойства
Гомологический ряд алканов
Алканы (предельные или насыщенные углеводороды, парафины) – углеводороды, атомы углерода в которых соединены простыми связями. Общая формула:  .
.
Соотношение числа атомов водорода и углерода в молекулах алканов максимально по сравнению с молекулами углеводородов других классов.
Поскольку, все валентности углерода заняты либо углеродами, либо водородами, как правило, химические свойства алканов не очень ярко выражены, поэтому их еще называют предельными или насыщенными углеводородами. И существует еще более древнее название, лучше отражающее их относительную, конечно, химическую инертность – парафины, что переводится как «лишенные сродства».
Строение молекул
Атомы углерода в алканах находятся в состоянии  – гибридизации, и молекулу алканов можно представить как набор тетраэдрических структур углерода, связанных между собой и с водородам.
– гибридизации, и молекулу алканов можно представить как набор тетраэдрических структур углерода, связанных между собой и с водородам.
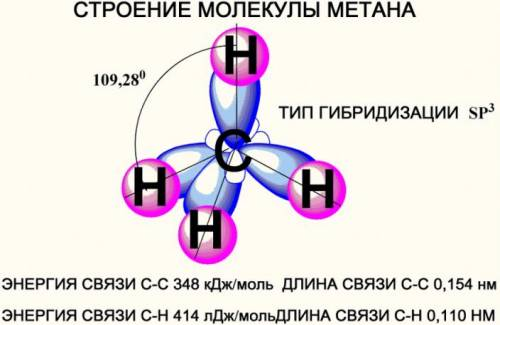
Тетраэдрическое строение метана
 -связи между атомами
-связи между атомами  и
и  прочные, практически неполярные (очень мало полярные).
прочные, практически неполярные (очень мало полярные).
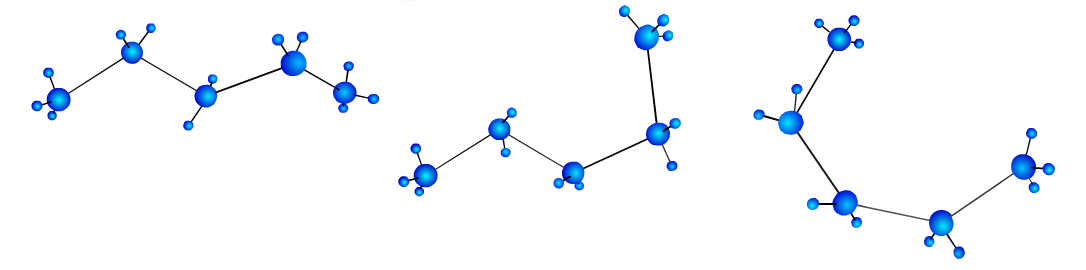
Атомы вокруг простых связей постоянно вращаются. Поэтому молекулы алканов могут принимать разные формы. При этом длина связи и угол между связями остаются постоянными. Формы, переходящие друг в друга за счет вращения молекулы вокруг  -связей, называют конформациями молекулы.
-связей, называют конформациями молекулы.
Номенклатура алканов
Первые четыре члена ряда алканов имеют исторически сложившиеся названия. Названия неразветвленных алканов с пятью и более атомами углерода в молекуле, образованы от греческих числительных, отражающих это число атомов углерода.
Суффикс -ан показывает принадлежность вещества к насыщенным соединениям.
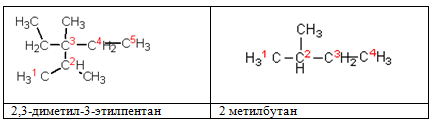
Составляя названия разветвленных алканов по номенклатуре ИЮПАК, в качестве основной цепи выбирают цепь, содержащую максимальное число атомов углерода. Основную цепь нумеруют таким образом, чтобы заместители получили наименьшие номера. Если цепей одинаковой длины несколько, то главной выбирают цепь, содержащую наибольшее число заместителей.
Физические свойства алканов
Температуры плавления и кипения в целом увеличиваются с увеличением числа атомов  в молекуле. Первые представители ряда алканов – газы при н.у., алканы, содержащие от 5 до 15 атомов
в молекуле. Первые представители ряда алканов – газы при н.у., алканы, содержащие от 5 до 15 атомов  – обычно жидкости, свыше 15 атомов
– обычно жидкости, свыше 15 атомов  – твердые вещества.
– твердые вещества.
Неразветвленные изомеры имеют более высокую температуру кипения, чем разветвленные (причина – разные силы межмолекулярного взаимодействия). Температуры плавления зависят, кроме того, от плотности упаковки молекул в кристалле.
Газообразные и твердые алканы не пахнут, жидкие алканы обладают характерным “бензиновым” запахом.
Все алканы бесцветны, легче воды и нерастворимы в ней. Алканы хорошо растворяются в органических растворителях, жидкие алканы (пентан, гексан) сами широко используются как растворители.
Химические свойства алканов
Алканы относятся к углеводородам, в которых отсутствуют кратные связи. Одно из названий углеводородов этого ряда – парафины, обозначает их химическую пассивность. Поэтому химические свойства алканов определяются таким образом:
1. Из-за предельности алканов реакции присоединения для них нехарактерны.
2. Из-за прочных связей  и
и  (короткие и практически неполярные) следует малая реакционная способность (не реагируют с кислотами, щелочами,
(короткие и практически неполярные) следует малая реакционная способность (не реагируют с кислотами, щелочами,  и т.п.)
и т.п.)
3. Неполярность связей свидетельствует о том, что реакции могут проходить по свободнорадикальному механизму.
Основной тип реакций – радикальное замещение (radical substitution)  .
.
Разорвать связь можно при помощи нагревания или УФ-излучения. Обычно реакции алканов идут при повышенных температурах или на солнечном свету.
Реакция галогенирования.
При хлорировании атом  в молекуле метана замещается на атом
в молекуле метана замещается на атом  . В избытке хлора происходит дальнейшее замещение:
. В избытке хлора происходит дальнейшее замещение: ;
; ;
; ;
; .
.
Реакция нитрования.
По механизму радикального замещения протекает реакция нитрования алканов в газовой фазе (реакция Коновалова). Условия – повышенные температура и давление.
В парообразном состоянии азотная кислота разлагается: .
.
Оксид азота (IV) является радикалом  . Он атакует молекулу алкана.
. Он атакует молекулу алкана.
Итоговая реакция: .
.
Горение алканов
Смесь метана с кислородом (в объёмном соотношении 1:2) или с воздухом (1:10) при поджигании сгорает со взрывом. Поэтому смеси метана, пропана, этана, бутана с воздухом очень опасны. Они иногда могут образоваться в шахтах, в мастерских, в жилых помещениях. С этими газами нужно проявлять осторожность при применении.












