Краткий конспект подготовки к ЗНО по физике №17 "Тепловой баланс"
Конспект 17. Тепловой баланс
1. Способы изменения внутренней энергии
Способы изменения внутренней энергии:
1) За счет совершения работы: 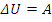
2) Путем теплообмена: 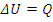
Определение. Теплообмен – процесс изменения внутренней энергии без совершения работы над телом.
Виды теплообмена:
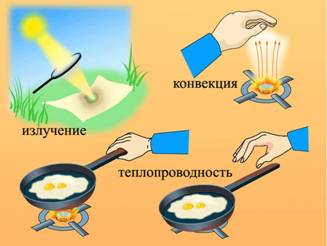
1) Определение. Теплопроводность – передача тепла от более нагретых частей тела к менее нагретым или передача тепла при контакте тел.
Примеры: нагрев посуды на плите, охлаждение продуктов в холодильнике и т.п.
2) Определение. Конвекция – перенос теплоты струями жидкости или газа.
Примеры: система кондиционирования и отопления помещений, нагрев воды в кастрюле и т.п.
Виды конвекции:
– естественная – самопроизвольное перемешивание слоев жидкости или газа вследствие того, что более теплые слои поднимаются, а более холодные опускаются. Например, обогрев комнаты при помощи калорифера
– принудительная – перемешивание слоев вещества под действием внешних сил. Например, перемешивание горячего чая
3) Определение. Тепловое излучение (электромагнитное) – передача тепла путем излучения электромагнитных волн (преимущественно инфракрасного диапазона), может проходить без наличия среды.
Примеры: нагрев тел от солнца, использование технологии приема теплового излучения в некоторых видах приборов ночного видения и в тепловизорах.
2. Агрегатные состояния веществ
Основные агрегатные состояния веществ:
1) Твердое – тело сохраняет форму и объем. Частицы вещества совершают колебания вокруг определенных положений и практически не перемещаются в веществе, расположение частиц плотное.
2) Жидкое – тело не сохраняет форму, но сохраняет объем. Частицы вещества не имеют определенного положения, но и не могут абсолютно свободно перемещаться, т.к. между ними действуют достаточно большие силы притяжения, расположение частиц достаточно плотное. Жидкость, налитая в сосуд в гравитационном поле, принимает его форму, но не обязательно занимает весь объем.
3) Газообразное – тело не сохраняет ни форму, ни объем. Частицы вещества движутся хаотически и слабо взаимодействую друг с другом, расположение частиц свободное. Газ занимает весь объем сосуда, в котором находится.

Определение. Агрегатный переход (превращение) – процесс перехода вещества из одного агрегатного состояния в другое.
Виды изменения внутренней энергии:
1) Без агрегатного перехода – нагревание и охлаждение
2) С агрегатным переходом:
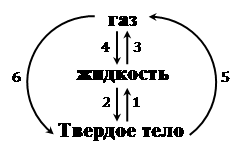
1 – плавление
2 – отвердевание (кристаллизация)
3 – парообразование: испарение или кипение
4 – конденсация
5 – сублимация (возгонка) – переход из твердого состояния в газообразное, минуя жидкое
6 – десублимация – переход из газообразного состояния в твердое, минуя жидкое
3. Уравнение теплового баланса
Рассмотрим какие количества теплоты необходимы для протекания различных видов изменения внутренней энергии.
1) Нагревание и охлаждение без агрегатного перехода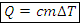 – количество теплоты нагревания/охлаждения тела, Дж
– количество теплоты нагревания/охлаждения тела, Дж
Где c – удельная теплоемкость тела (табл.), Дж/(кг∙К)
m – масса тела, кг
∆t – разность температур, К
Замечание. Чем выше удельная теплоемкость тела, тем больше необходимо тепла, чтобы нагреть его на 1 К.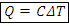 – количество теплоты нагревания/охлаждения тела (редко используемая формула), Дж
– количество теплоты нагревания/охлаждения тела (редко используемая формула), Дж
Где С=cm – теплоемкость тела, Дж/К
2) Парообразование и конденсация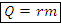 – количество теплоты парообразования, Дж
– количество теплоты парообразования, Дж
Где r – удельная теплота парообразования (табл.), Дж/(кг )
Замечание. Оба процесса начинаются при определенной температуре, температуре кипения, которая равна температуре конденсации (табл.).
Замечание. Во время агрегатного перехода температура постоянна.
3) Плавление и кристаллизация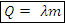 – количество теплоты плавления, Дж
– количество теплоты плавления, Дж
Где λ - удельная теплота плавления, Дж/(кг )
Замечание. Оба процесса начинаются при определенной температуре, температуре плавления, которая равна температуре кристаллизации (табл.).
4) Сгорание топлива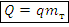 – количество теплоты сгорания топлива, Дж
– количество теплоты сгорания топлива, Дж
Где q – удельная теплота сгорания топлива (табл.), Дж/(кг ) – масса топлива, кг
– масса топлива, кг
Принцип теплового баланса – тела, находящиеся в замкнутой системе, с течением времени приходят к одинаковой температуре.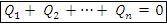 – уравнение теплового баланса
– уравнение теплового баланса
Знаки количества теплоты:
Q>0 – тело получает тепло
Q<0 – тело отдает тепло
Замечание. Иногда используется следующая форма записи уравнения теплового баланса: 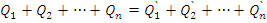 , где
, где 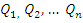 – полученное тепло,
– полученное тепло,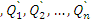 – отданное тепло.
– отданное тепло.
Замечание. Калориметр – теплоизолированный прибор для измерения количества теплоты (аналог термоса).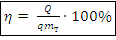 – КПД нагревателя, % или ед.
– КПД нагревателя, % или ед.
Где Q – суммарное полезное количество теплоты, Дж
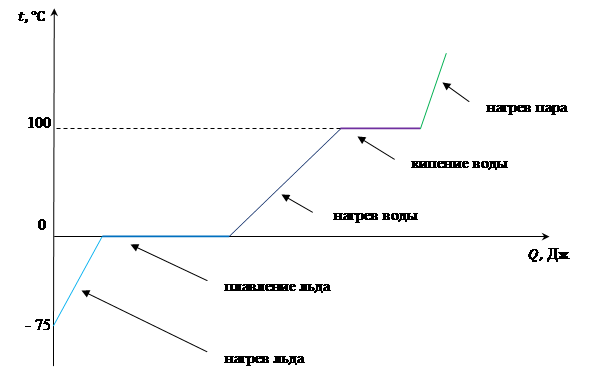
График зависимости температуры вещества от полученного им тепла на примере воды