Онлайн-урок №29 "Аміни"
Онлайн-урок №29 "Аміни"
20.05.2016 в 18.30
Конспекти до уроку:
Амины – это органические соединения, в состав которых входит трехвалентный атом азота. Амины можно представить как органические производные аммиака.
Аминогруппа – функциональная группа аминов. Состоит из трехвалентного атома азота и связанных с ним атомов водорода. Например:  .
.
Классификация аминов
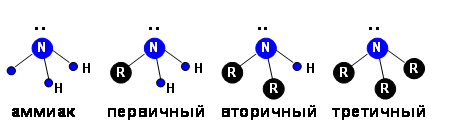
Первичный амин – это амин, в котором атом азота образует одну связь с углеводородным радикалом и две с атомами водорода.
Вторичный амин – это амин, в котором атом азота образует две связи с углеводородными радикалами и одну с атомом водорода.
Третичный амин – это амин, в котором атом азота образует три связи с углеводородными радикалами.
Существуют циклические амины. Например: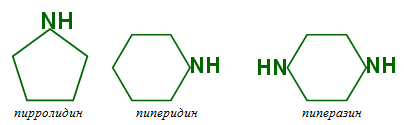
пирролидин пиперидин пиперазин
Подобно многоатомным спиртам, существуют и амины, имеющие несколько аминогрупп: этилендиамин
этилендиамин кадаверин
кадаверин спермин
спермин
Номенклатура аминов
Для построения названий первичных аминов используется суффикс «амин» (или приставка «амино»). метанамин
метанамин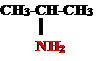 пропанамин-2
пропанамин-2 гександиамин-1,6
гександиамин-1,6
Эта номенклатура неудобна для вторичных и третичных аминов. Их названия строятся, исходя из корня “амин”. К нему присоединяются приставки, обозначающие радикалы. Они перечисляются в алфавитном порядке. Первичные амины также можно называть таким образом. метилэтиламин
метилэтиламин диметиламин
диметиламин метиламин
метиламин
Изомерия аминов
1. Скелетная изомерия: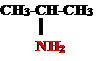 пропанамин-2, изопропиламин
пропанамин-2, изопропиламин пропанамин-1, н-пропиламин
пропанамин-1, н-пропиламин
2. Изомерия положения и взаимного положения аминогрупп: бутандиамин-1,4, путресцин
бутандиамин-1,4, путресцин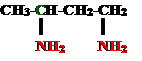 бутандиамин-1,3, изопутресцин
бутандиамин-1,3, изопутресцин
3. Оптическая изомерия:
В молекуле изопутресцина (см. выше) есть асимметрический атом углерода. Он выделен зеленым цветом и отвечает за существование двух разных оптических изомеров этого соединения.
Изомерия, связанная с перераспределением атомов углерода между углеводородными радикалами: н-пропиламин
н-пропиламин метилэтиламин
метилэтиламин триметиламин
триметиламин
Физические свойства аминов
Амины имеют резкий запах, с одной стороны, похожий на запах аммиака, а с другой – на запах гниющей рыбы.
Полярность связи  и наличие водородных связей:
и наличие водородных связей:
1. Большинство аминов – жидкости (только метиламин, этиламин, диметиламин и триметиламин – газы).
2. Хорошая растворимость в воде.
Растворимость третичных аминов меньше, чем вторичных и первичных, потому что у третичных аминов отсутствуют атомы водорода при атоме азот, нет сильно полярной связи  .
.
Амины с большими углеводородными радикалами растворяются плохо, потому что малополярные фрагменты алканов гидрофобны.
Химические свойства аминов
Амины сходны по строению с аммиаком и с алканами. Поэтому они проявляют схожие свойства. Но аминогруппа влияет на углеводородный радикал, а он – на аминогруппу.
Горение аминов.
Амины загораются на воздухе легче, чем аммиак. ;
; .
.
Основные свойства.
Первичные, вторичные и третичные амины обязательно содержат неподеленную электронную пару, как и полагается трехвалентному азоту. То есть амины в растворе проявляют основные свойства или их растворы являются основаниями.
Подобно аммиаку, амины проявляют свойства оснований: ;
; .
.
С кислотами аммиак образует соли аммония, а амины – алкиламмония: (бромид аммония)
(бромид аммония) (бромид этиламмония)
(бромид этиламмония)
Анилин
Простейший представитель класса ароматических аминов – анилин. Это маслянистая жидкость, немного растворимая в воде.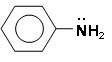
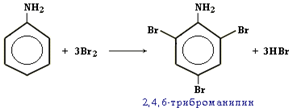
Анилин реагирует с бромной водой, при этом сразу образуется
2,4,6-триброманилин – белый осадок (качественная реакция на анилин и другие амин бензолы).
Вспомним: бензол взаимодействует с бромом только в присутствии катализатора.
Применение анилина и аминов
Из продуктов окисления анилина получают анилиновые красители, отличающиеся стойкостью и яркостью.
Из анилина и аминов получают применяемые для местного наркоза анестезин и новокаин; противобактериальное средство стрептоцид; популярное обезболивающее и жаропонижающее средство парацетамол: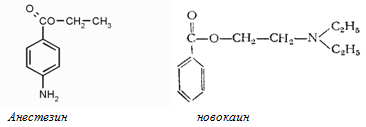
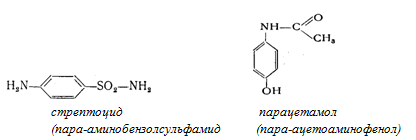
Анилин и амины – сырье для производства пластмасс, фотореактивов, взрывчатых веществ. Взрывчатое вещество гексил (гексанитродифениламин):
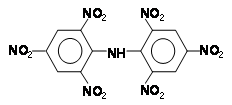
Получение анилина и аминов
1. Нагревание галогеналканов с аммиаком или менее замещенными аминами (реакция Гофмана). (правильнее
(правильнее  );
);
2. Вытеснение аминов из их солей нагреванием со щелочами: .
.
3. Восстановление нитро соединений (реакция Зинина): ;
;
Тести до уроку:
Онлайн-тест подготовки к ЗНО по химии №46 "Амины"
Корисні посилання:
Строение и номенклатура аминов
Получение гидроксида диметиламмония и его свойства












