Онлайн-урок №29 "Строение атома. Строение ядра атома. Ядерные реакции."
Онлайн-урок №29 "Строение атома. Строение ядра атома. Ядерные реакции."
10.05.2016 в 18.30
Конспекты к уроку:
Конспект 37. Строение атома. Элементы теории относительности.
Тема: Строение атома и атомного ядра, СТО
1. Строение атома
История выдвижения гипотез о строении атома:
1) Древнегреческий философ Демокрит предполагал, что вещество состоит из атомов. Атом в переводе с древнегреческого – «неделимый»;
2) Д.Томсон в 1904 г. предлагает, т.н. «пудинговую модель атома» или «модель кекса». В ней атом представляет собой цельную субстанцию с положительным зарядом, которая распределена по всему объему атома, а в ней находятся вкрапления электронов подобно изюму в кексе;
3) Э. Резерфорд в 1911 г. публикует статью, в которой предлагает свою «планетарную модель атома», которая максимально близка к современным представлениям об атоме.
Идея опыта Резерфорда по исследованию строения атома заключалась в рассеивании α-частиц (ядер атомов гелия 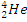 ) при прохождении тонких слоев вещества (золотая фольга).
) при прохождении тонких слоев вещества (золотая фольга).
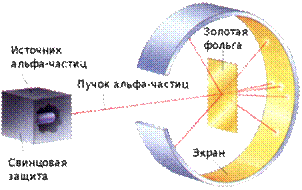
Опыты заключались в подсчете вспышек на люминесцентном экране, вызванных ударом α-частиц. Поток частиц направлялся на тонкую золотую фольгу, окруженную люминесцентным экраном, после прохождения фольги на экране с помощью микроскопа наблюдали вспышки. В результате бомбардировки α-частицами золотой фольги большинство частиц отклонялось на небольшой угол, а очень малая часть отражалась назад.
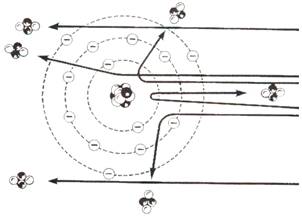
| Схема опыта Резерфорда | Отклонение α-частиц в атоме |
 |
 |
Основные результаты опытов Резерфорда:
1) Положительный заряд атома сконцентрирован в небольшом тяжелом ядре;
2) На большом расстоянии от ядра вращаются отрицательно заряженные электроны.
Замечание. В нейтральном атоме суммарный заряд электронов равен по модулю, но противоположен по знаку заряду ядра (количество электронов равно количеству протонов).
Замечание. С точки зрения классической электродинамики атом по модели Резерфорда не мог бы долго существовать из-за излучения ЭМВ электронами. Выход из противоречия этой модели законам электродинамики был найден в 1913 г. Н. Бором.
Постулаты Бора:
1) Постулат стационарных состояний – в атоме существуют определенные стационарные состояния, при которых он не излучает энергии, этим состояниям соответствуют стационарные орбиты вращения электронов, на которых они не излучают ЭМВ. Каждая орбита характеризуется определенной энергией;
2) Правило частот – при переходе электрона с одной орбиты на другую поглощается/излучается фотон с энергией, которая равна разности энергий на орбитах.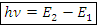 – энергия поглощенного/излученного фотона, Дж
– энергия поглощенного/излученного фотона, Дж
Где 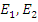 – энергии электрона на орбитах, между которыми совершался переход, Дж
– энергии электрона на орбитах, между которыми совершался переход, Дж
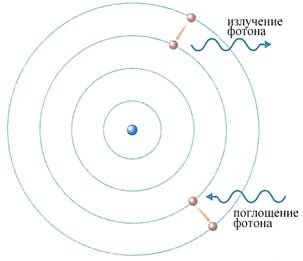
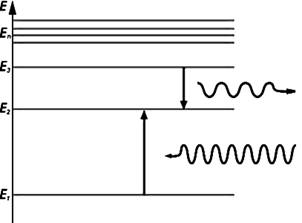
Замечание. При поглощении фотона происходит переход электрона на более высокую орбиту, при излучении – на более низкую.
 |
 |
Замечание. В связи с тем, что атомы различных веществ способны излучать/поглощать определенный уникальный для них набор частот ЭМИ (спектры), стали выделять несколько видов таких спектров.
Типы спектров:
1) Сплошной спектр состоит из набора всех длин волн, излучается при нагревании жидких и твердых тел, а также сильно сжатых газов (как Солнце).
2) Линейчатый спектр состоит из набора отдельных спектральных линий и возникает при нагревании атомарных газов.
3) Полосатый спектр состоит из полос плотно расположенных спектральных линий, полосы отделены темными участками, излучается молекулярными газами.
Пример практического использования: спектральный анализ – метод идентификации веществ по спектрам.
2. Элементы специальной теории относительности (СТО)
Постулаты теории относительности Эйнштейна:
1) Все процессы природы протекают во всех инерциальных системах отсчета (ИСО) одинаково;
2) Скорость света в вакууме 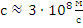 является абсолютной величиной, т.е. одинакова в любой ИСО и не зависит от скорости движения источника.
является абсолютной величиной, т.е. одинакова в любой ИСО и не зависит от скорости движения источника.
Замечание. Явления, которые имеют место при скоростях движения, близких к скорости света, принято назвать релятивистскими.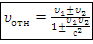 – релятивистский закон сложения скоростей, м/с
– релятивистский закон сложения скоростей, м/с
Где 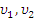 – скорости двигающихся относительно друг друга тел, м/с
– скорости двигающихся относительно друг друга тел, м/с
Замечание. Достигнуть и превысить скорость света в вакууме невозможно, единственная частица, которая ее достигает, это фотон.
Релятивистские эффекты: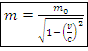 – увеличение массы, кг
– увеличение массы, кг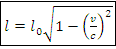 – сокращение длины объекта, м
– сокращение длины объекта, м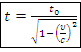 – замедление времени, с
– замедление времени, с
Где 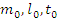 – масса покоя, собственная длина, собственное время в ИСО, принятой за неподвижную, а
– масса покоя, собственная длина, собственное время в ИСО, принятой за неподвижную, а 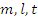 – относительные величины в движущейся ИСО.
– относительные величины в движущейся ИСО.
Замечание. Согласно СТО между массой и энергией существует связь и возможность взаимопревращения.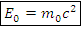 – энергия покоя, Дж
– энергия покоя, Дж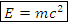 – полная релятивистская энергия, Дж
– полная релятивистская энергия, Дж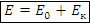 – связь полной релятивистской энергии с энергией покоя, Дж
– связь полной релятивистской энергии с энергией покоя, Дж
Где 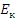 – кинетическая энергия тела, Дж
– кинетическая энергия тела, Дж
Замечание. 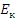 нельзя выражать по формуле классической механики.
нельзя выражать по формуле классической механики.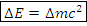 – изменение энергии тела, Дж
– изменение энергии тела, Дж
Конспект 38. Строение атомного ядра. Ядерные реакции. 3. Строение атомного ядра
Строение ядра атома (нуклоны):
1) Протоны – положительно заряженные частицы (их заряд равен элементарному заряду, т.е. модулю заряда электрона), их количество равно порядковому номеру элемента в таблице Менделеева (обозначается Z – зарядовое число);
2) Нейтроны – незаряженные частицы, их количество определяется по формуле N=A-Z, где A – округленное до целых значение атомной массы (нуклонное число).
Замечания:
1) Общее обозначение ядра данного элемента: 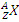 , где X – обозначение элемента в таблице Менделеева;
, где X – обозначение элемента в таблице Менделеева;
2) Обозначения элементарных частиц: 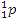 – протон,
– протон, 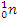 – нейтрон,
– нейтрон, 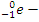 электрон;
электрон;
3) Массы микрочастиц удобно вычислять в а.е.м., 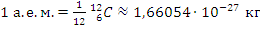 ;
;
4) Массы протона и нейтрона примерно равны 1 а.е.м., их приблизительные значения являются мировыми константами;
5) Массой электрона часто принято пренебрегать по сравнению с массами протона и нейтрона.
Определение. Изотопы – элементы с одинаковым количеством протонов Z и различным количеством нейтронов N в ядре. Свойства различных изотопов одного и того же элемента могут сильно отличатся.
Примеры изотопов водорода: 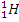 – протий,
– протий, 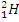 – дейтерий,
– дейтерий, 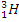 – тритий.
– тритий.
Определение. Дефект масс ядра (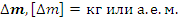 ) – разница между суммой масс нуклонов ядра в свободном состоянии и массой покоя самого ядра. Масса ядра всегда меньше суммы масс его нуклонов.
) – разница между суммой масс нуклонов ядра в свободном состоянии и массой покоя самого ядра. Масса ядра всегда меньше суммы масс его нуклонов.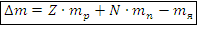 – дефект масс ядра, кг или а.е.м.
– дефект масс ядра, кг или а.е.м.
Где 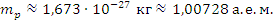 – масса покоя протона
– масса покоя протона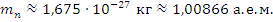 – масса покоя нейтрона
– масса покоя нейтрона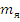 – масса покоя ядра (табл.), кг или а.е.м.
– масса покоя ядра (табл.), кг или а.е.м.
Определение. Энергия связи ядра (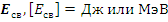 ) – энергия, которая необходима для расщепления ядра на входящие в него нуклоны.
) – энергия, которая необходима для расщепления ядра на входящие в него нуклоны.
Энергия связи ядра: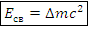 – Дж (∆m в кг)
– Дж (∆m в кг)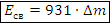 – МэВ (∆m в а.е.м.)
– МэВ (∆m в а.е.м.)
Замечание. Часто для измерения энергий в микромире используется единица измерения электронвольт: 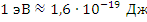 , соответственно
, соответственно 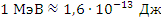 .
.
Определение. Удельная энергия связи атомных ядер (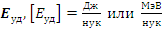 ) – энергия связи, приходящаяся на один нуклон.
) – энергия связи, приходящаяся на один нуклон.
Замечание. Это средняя характеристика стойкости ядра к самопроизвольному распаду, чем эта энергия меньше, тем ядро менее стабильно. Последним стабильным ядром в таблице Менделеева является свинец.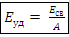 – удельная энергия связи ядра,
– удельная энергия связи ядра, 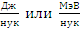
Определение. Ядерные реакции – искусственные превращения атомных ядер, обусловленные взаимодействием с различными частицами или с другими ядрами.
Пример записи ядерной реакции: 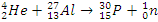 .
.
Правила составления ядерных реакций:
1) Сумма нуклонных чисел A у элементов, вступающих в реакцию, и у ее продуктов равна;
2) Сумма протонных (зарядовых) чисел Z у элементов, вступающих в реакцию, и у ее продуктов равна (закон сохранения заряда);
3) Неизвестный элемент определяется зарядовым числом по таблице Менделеева, проверяется соответствие порядкового номера и названия элемента.
Замечание. В результате протекания ядерных реакций наблюдается дефект масс ядерной реакции и выделение либо поглощение энергии.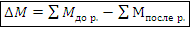 – дефект масс ядерной реакции, кг или а.е.м.
– дефект масс ядерной реакции, кг или а.е.м.
Варианты результатов ядерных реакций:
1) Энергия выделяется, если ∆M>0 – реакция экзоэнергетическая;
2) Энергия поглощается, если ∆M<0 – реакция эндоэнергетическая.
Энергетический выход ядерной реакции: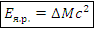 – Дж (∆M в кг)
– Дж (∆M в кг)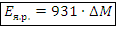 – МэВ (∆M в а.е.м.)
– МэВ (∆M в а.е.м.)
Определение. Радиоактивность – способность атомов некоторых химических элементов к самопроизвольному излучению.
Замечание. Э. Резерфорд обнаружил, что радиоактивное излучение состоит из α-частиц и β-частиц, позже было еще обнаружено γ-излучение, Ф. Содди сформулировал правила смещения.
Правила смещения для радиоактивного распада:
1) Во время α-распада нуклонное число ядра атома уменьшается на 4, а протонное – на 2, в результате образуется ядро элемента, порядковый номер которого в периодической таблице на 2 единицы меньше, чем порядковый номер исходного элемента.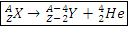
2) Во время β-распада нуклонное число ядра атома остается неизменным, а протонное увеличивается на 1, в результате образуется ядро элемента, порядковый номер которого в периодической таблице на 1 единицу больше, чем порядковый номер исходного элемента.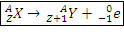
Замечание. Проникающие способности излучения: α-частицы задерживаются листом бумаги, β-частицы – пластиной алюминия толщиной несколько миллиметров, γ-излучение ослабляется свинцовой пластинкой толщиной 1 см примерно в два раза.
Счетчик Гейгера – прибор для регистрации ионизирующих частиц, в основе принципа работы которого лежит газовый разряд, возникающий из-за ионизации электронным ударом.
Определение. Период полураспада (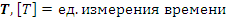 ) – время, за которое распадается половина радиоактивных ядер.
) – время, за которое распадается половина радиоактивных ядер.
Закон радиоактивного полураспада: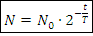
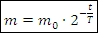
Где N – количество оставшихся ядер, ед.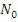 – начальное количество ядер, ед.
– начальное количество ядер, ед.
m – оставшаяся масса вещества, кг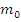 – начальная масса вещества, кг
– начальная масса вещества, кг
t – время распада, ед. измерения времени
T – период полураспада, ед. измерения времени
Замечание. Количество распавшихся ядер 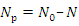 .
.
Тесты к уроку:
Онлайн-тест подготовки к ЗНО по физике №49 «Строение атома. Элементы теории относительности»
Онлайн-тест подготовки к ЗНО по физике №50 "Строение ядра атома. Ядерные реакции"
Онлайн-тест подготовки к ЗНО по физике №51 «Контрольная работа разделу «Квантовая физика. Элементы теории относительности»»
Онлайн-тест подготовки к ЗНО по физике №52 «Зачет по теории разделам «Колебания и волны», «Оптика», «Квантовая физика. Элементы теории относительности»»
Полезные ссылки:












